口罩出口美國及歐洲要什么認證?目前國內(nèi)疫情趨于緩和,歐洲、意大利、日本、韓國等感染人數(shù)持續(xù)上升,伊朗以極高的致死率引發(fā)全球關(guān)注。鑒于此,口罩商機很快轉(zhuǎn)移到了國外,口罩出口,成為如今疫情下的熱門生意。
美國口罩標(biāo)準及認證要求
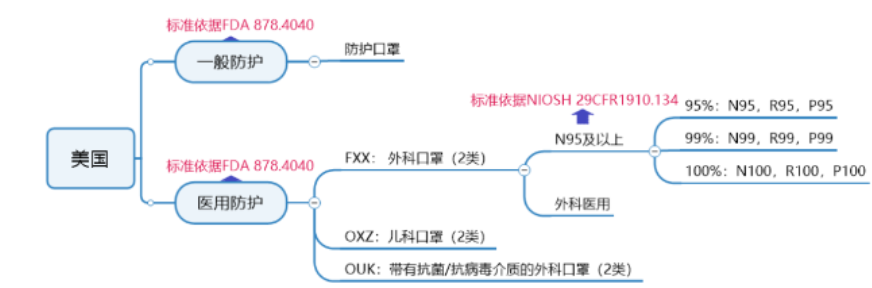
美國一般防護口罩認證要求:
按照美國FDA醫(yī)療做認證,流程為:
①填寫申請表格,信息確認;②獲取PIN碼,交付年費;
③下發(fā)注冊號;
④產(chǎn)品出口。
美國醫(yī)用外科口罩認證要求:
按照美國FDA醫(yī)療Ⅱ類做認證,流程為:①產(chǎn)品測試(性能測試、生物學(xué)測試);②準備510K文件,提交FDA評審;
③FDA發(fā)510K批準信;④完成工廠注冊和機器列名;
⑤產(chǎn)品出口。
美國醫(yī)用N95及以上9種口罩認證要求:
按照NIOSH認證標(biāo)準,企業(yè)需寄送樣品至NIOSH實驗室實施測試,同時提交技術(shù)性資料(包括質(zhì)量體系部分資料)至NIOSH文審,文審和測試都通過后,NIOSH核發(fā)批
歐盟口罩標(biāo)準及認證要求
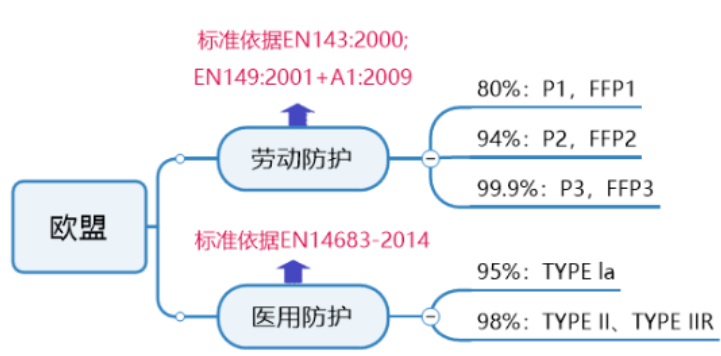
歐盟一般防護口罩認證要求:
個人防護口罩的歐洲標(biāo)準是EN149及EN143,防護口罩需要滿足歐盟個人防護設(shè)備指令(PPE)的要求,審核企業(yè)質(zhì)量管理體系和CE技術(shù)文檔,審核通過后可獲得PPE法規(guī)的CE證書。
歐盟醫(yī)用防護口罩認證要求:
醫(yī)用口罩對應(yīng)的歐洲標(biāo)準是EN14683,按照醫(yī)療器械法規(guī)2017/745/EU的要求,口罩產(chǎn)品可以按照一類器械進行管理。依據(jù)產(chǎn)品是無菌或非無菌狀態(tài)提供,認證模式有所差別。
澳大利亞&新西蘭口罩標(biāo)準及認證要求
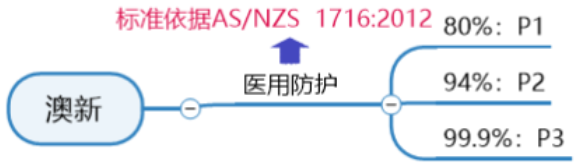
澳新醫(yī)用防護口罩認證要求:
AS/NZS1716:2012是澳大利亞和新西蘭的呼吸保護裝置標(biāo)準。該標(biāo)準規(guī)定了防顆粒口罩制造過程中必須使用的程序和材料,以及確定的測試和性能結(jié)果,以確保其使用安全。
韓國口罩標(biāo)準及認證要求
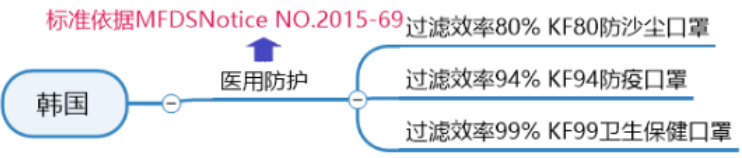
韓國醫(yī)用口罩認證標(biāo)準:
韓國的口罩標(biāo)準KF(Korean filter)系列,是由韓國的食品藥品管理部門(Ministry of Food and Drug Safety,MFDS)發(fā)布的韓國主流口罩標(biāo)準
(Regulations on the Approval,Notification,and Evaluation of Quasi-Drugs)。
日本口罩標(biāo)準及認證要求
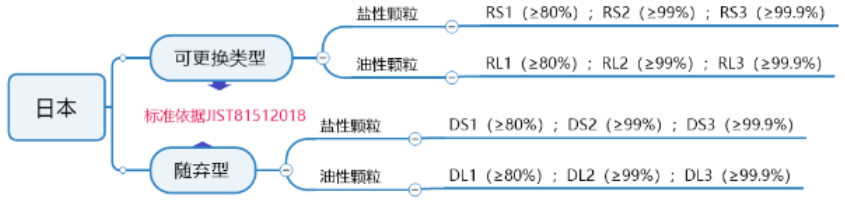
日本JIST81512018標(biāo)準是呼吸保護裝置的標(biāo)準,也是日本厚生勞動省(MHLW)驗證標(biāo)準,出口日本需要做此認證。
歡迎您直接來電咨詢我司工作人員,獲得詳細的費用報價與周期等信息。
上一篇:美國FCC認證和國內(nèi)3c認證有什么區(qū)別?
下一篇:面罩電商質(zhì)檢報告GB32166辦理流程
- 海灣七國GCC認證常見疑問解析
- NCCS宣布光網(wǎng)絡(luò)終端和光線路終端安全認證的強制日期
- 國家認監(jiān)委批準《汽車芯片認證審查 通用技術(shù)要求》等5項認證認可行業(yè)標(biāo)準
- 歐盟擴大REACH附錄XVII 多環(huán)芳烴(PAHs)的限制 范圍!
- 歐盟發(fā)布化學(xué)和相關(guān)活動的實驗裝置標(biāo)準EN 71-4:2020+A1:2025
- 加拿大ISED認證收費標(biāo)準調(diào)整要注意什么
- ECHA發(fā)布REACH PFAS限制提案最新進展
- 國家衛(wèi)生健康委發(fā)布5項食品接觸材料新標(biāo)準及1項標(biāo)準修改單
- 服裝及鞋襪國際RSL管理(AFIRM)2025版限用物質(zhì)清單測試介紹
- 雙標(biāo)”+監(jiān)督辦法三重升級!2025食品標(biāo)簽新規(guī)亮點解析



